Wirtszell proteine (HCPs), die aus technischen Zellen in der bio pharmazeut ischen Produktion stammen, können möglicher weise die Produkt qualität, Wirksamkeit und Sicherheit beeinträchtigen. Daher stellt die HCP-Überwachung ein kritisches Qualitäts attribut (CQA) im Herstellungs prozess dar. Angesichts der großen Vielfalt der HCPs sind mehrere Erkennungs-und Identifikation stech niken erforderlich, um die globalen Regulierungs standards zu erfüllen.
1. HCP-Analyse-und Detektion stech no logie plattform (ELISA, LC-MS & 2D)
A. SHENTEK®HCP ELISA KitAuf eine bestimmte Technik zuges chnitten, um eine präzise und gezielte Erkennung zu gewährleisten.
B. HCP ELISA-Standards Rück verfolgbar keits system, um sicher zustellen, Assay Präzision und Zuverlässigkeit.
C. Genaue Bewertung der prozess spezifischen und risiko reichen HCPs und der Unterschiede der HCPs zwischen Chargen, wie z. B. präklinische und klinische Studien lose.
D. Identifizieren Sie Hochrisiko-HCPs mithilfe orthogonaler Techniken, um die HCP-ELISA-Einschränkungen für die Entwicklung von Bio prozessen zu ergänzen.
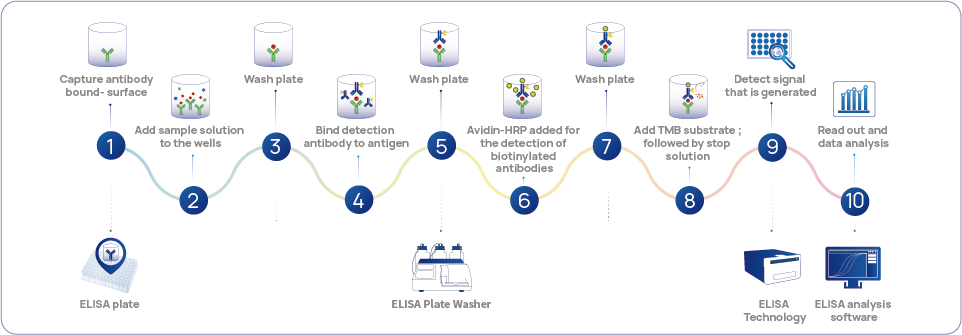
Abbildung 1 HCPs-Standard technologie-ELISA-Erkennungs workflow
2. HCP-Plattform für die Analyse von Antikörpern (IMBS-2D und IMBS/LC-MS)
A. IMBS®(Immuno magnetische Perlen trennung) Technologie basierend auf Antigen-Antikörper-magnetischen Perlen-Immun komplexen zur schnellen Trennung spezifischer Antigene.
B. 2D und LC-MS bieten eine präzise und objektive Darstellung des Matching-Grades zwischen Antikörpern und HCPs mit mehreren Winkeln.
C. Die HCP-Antikörper-Spezifität wird durch Abdeckung analyze an simulierten oder frühen Prozess proben gemessen.
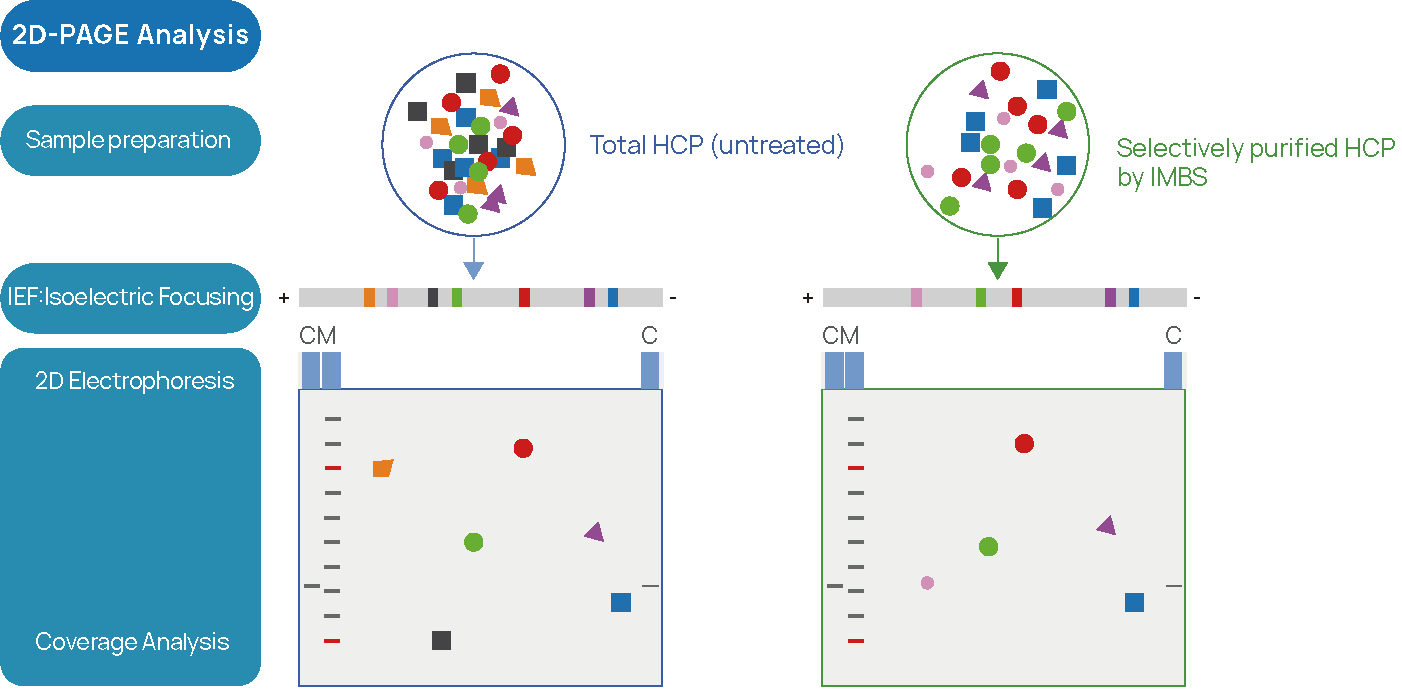
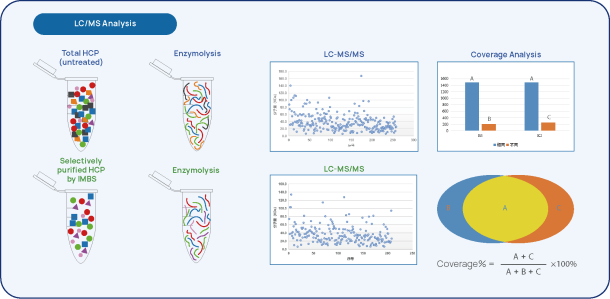
Abbildung 2 IMBS-2D und IMBS-LC/MS HCP-Antikörper-Abdeckung analyze
3. HCP-Plattform zur Herstellung polyklonaler Antikörper
A. Passen Sie Immun wege und Strategien für verschiedene Antigene an.
B. Überwachen Sie die Vorbereitung hochwertiger Antikörper mit präziser Antikörper charakterisierung während des gesamten Prozesses.
C. Eine standard isierte Multi-Mode-Plattform zur Vorbereitung von Antikörpern, um die Erzeugung von Antikörpern mit hoher Abdeckung srate und Wirksamkeit sicher zustellen.
D. Stellen Sie die Zuverlässigkeit und Vergleichbar keit des Erkennungs systems durch das Rück verfolgbar keits system von HCP-Referenz produkten sicher.
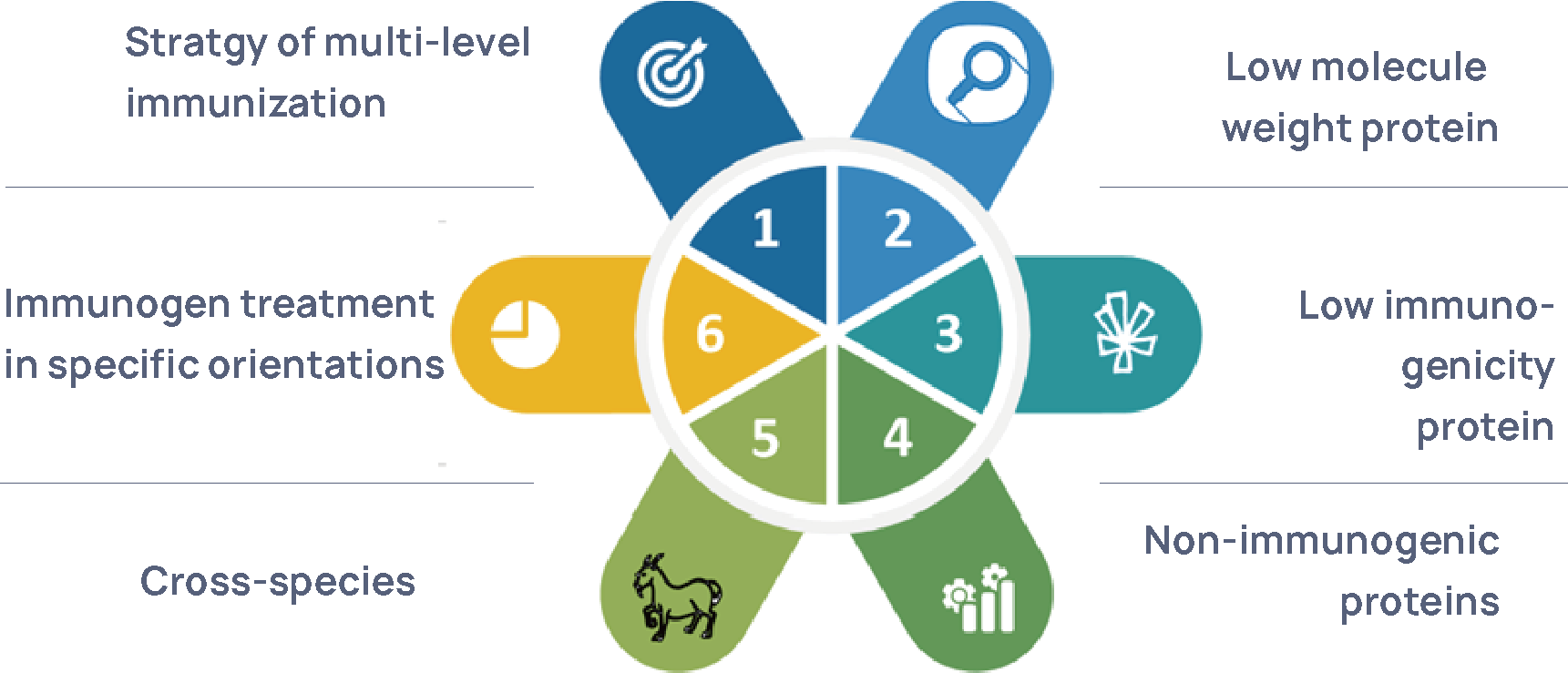
Abbildung 3 HCP-Plattform zur Herstellung polyklonaler Antikörper
4. Kunden spezifische HCP ELISA Kit Plattform
A. Umfassende Studien zu Rest-HCP-Standards (rHCP), um eine hervorragende Abdeckung und Spezifität zu erreichen.
B. Standard praxis der Rück verfolgbar keit von HCP-Referenz, um die Zuverlässigkeit von Immuno assays sicher zustellen.
C. Wirksame und intensive Strategien zur Herstellung von Antigen und Antikörpern für robuste Immunantwort und hochwertige polyklonale Antikörper.
D. Einhaltung des Qualitäts systems ISO13485, um die hochwertige Entwicklung des HCP-ELISA-Kits zu garantieren.
E. Einhaltung der Qualitäts standards CNAS/ISO10725 und GMP, um die Integrität des Dienstes und der Produkte sicher zustellen.
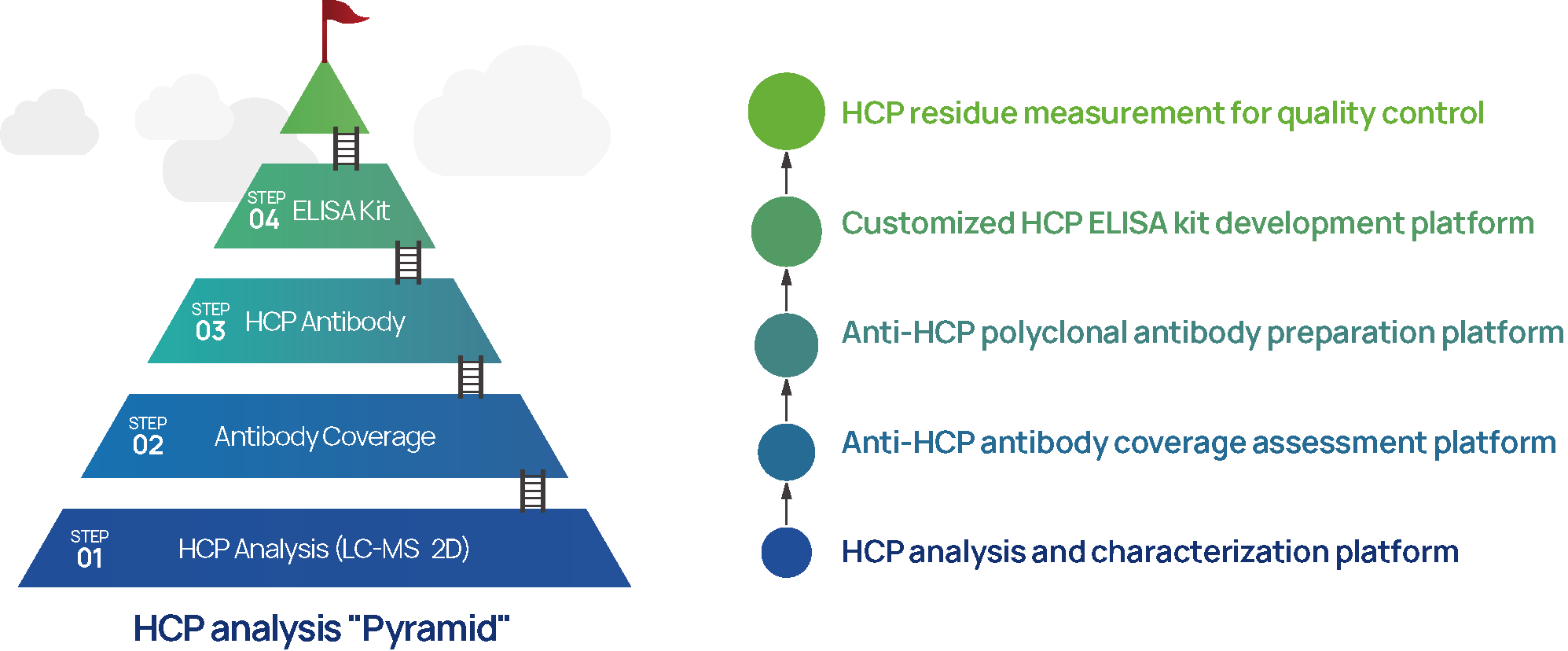
Abbildung 4: SHENTEK-Dienst plattformen für die Analyse von Rest wirts zellprotein