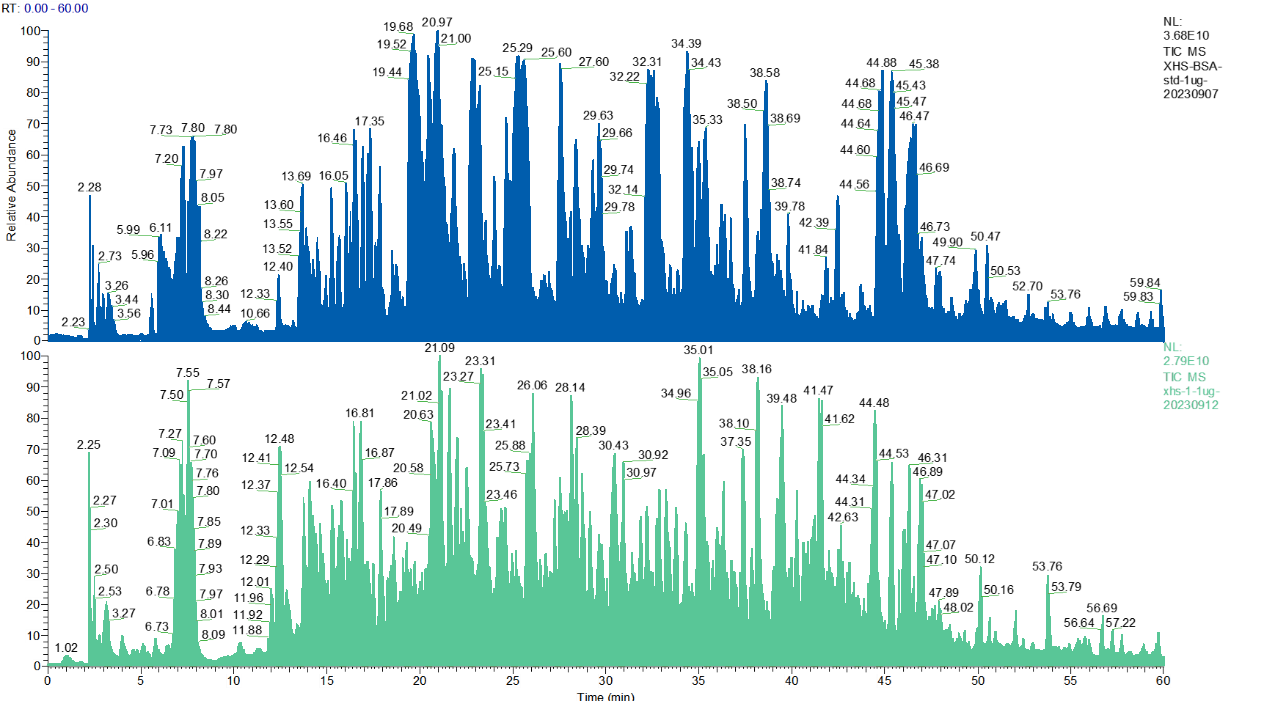
Rekombinante Proteine werden haupt sächlich in Wirtszellen wie Bakterien, Hefen, Säugetieren, Insekten oder Pflanzen zelllinien exprimiert. Während des Bioproduktion prozesses produzieren diese Wirtszellen auch Nebenprodukt proteine, die für normale Zell funktionen notwendig sind. Wenn Zellen Apoptose, Tod und Lyse erfahren, werden diese Nebenprodukt proteine in das Zellkultur medium freigesetzt. Folglich,Rest wirts zell proteinWerden zu kritischen prozess bedingten Verunreinigungen, die sich auf die klinische Sicherheit und Wirksamkeit auswirken können. Das US-amerikanische Pharma copeia schreibt vor, dass die HCP-Rückstands werte zwischen 1 und 100 ng/mg liegen sollten.
ELISA-Assays sind trotz einiger Einschränkungen die pharma ko peiale Methode zur HCP-Quant ifizierung. Zum Beispiel beträgt die Antikörper abdeckung in ELISA-Kits nur etwa 50%-80%, was bedeutet, dass sie nicht alle HCP-Typen abdecken kann. Darüber hinaus kann ELISA nur die Gesamtmenge an HCP messen und keine Informationen über die Arten und Mengen einzelner HCPs liefern. Branchen experten empfehlen daher die Verwendung von Massen spektrometrie zur genauen Identifizierung und quantitativen Analyse von HCPs als orthogonale Methode.
1. Bio prozess optimierung
Es werden vergleichende Studien von In-Process-Proben aus verschiedenen Routen durchgeführt, um die schrittweise Effizienz der HCP-Entfernung zu analysieren und dabei den optimalen Weg zu identifizieren. Da ELISA nur den Gesamt-HCP-Gehalt nachweisen kann, können einige HCPs mit hohem Gehalt, aber geringer Immun ogenität (von Antikörpern nicht erkannt) nicht effektiv überwacht werden. Daher wird empfohlen, Massen spektrometrie daten während der Prozessent wicklung für eine genauere Überwachung zu verwenden.
2. HCP-Analyse in den Endprodukten
Eine vergleichende Analyse von Arzneimittel substanzen aus verschiedenen Chargen wird durchgeführt, um die Stabilität der Bio verarbeitung zu bewerten. Diese Analyse in Kombination mit ELISA-Daten bewertet die verbleibenden HCP-Verunreinigungen weiter und reduziert die klinischen Risiken.