Bio logika werden aus den Wirten von Bakterien, Hefen, tierischen Zellen und kontinuier lichen Zelllinien exprimiert. Da biologische Produkte aus einem Zell substrat hergestellt werden, ist es unvermeidlich, dass in den Endprodukten verbleibende Wirtszell-DNA vorhanden ist. Es hat potenzielle Risiken für Immun ogenität, Onkogenität und Infekt iosität aufgrund der Tumor-oder virus bezogenen Gene in Durchgangs zelllinien. Rest-DNA hat ein potenziell hohes Sicherheits risiko und wird als kritisches Qualitäts merkmal angesehen. Derzeitige Agenturen, darunter die WHO, die EU und die FDA, begrenzten die akzeptierten Mengen an Rest-DNA (weniger als 10 ng oder 100 pg/Dosis). Unter den Methoden zum Nachweis von Rest-DNA wird qPCR aufgrund seiner Empfindlichkeit, Genauigkeit, Präzision und Zeiters parnis als die praktisch ste für die Rest-DNA-Quant ifizierung angesehen.
Da rDNA von einer Vielzahl von Wirten stammen kann, kann rDNA in verschiedenen Größen und physikalischen Formen existieren. unterschied liche Grenzwerte für DNA-Gehalt und-Größe können für die Aufsichts behörden akzeptabel sein, wenn sie durch wissenschaft liche Nachweise und eine solide Risiko bewertung gestützt werden. Das Niveau der Wirtszell-DNA-Residuen kann als Indikator für die Produkt konsistenz und Qualitäts kontrolle dienen. Der Nachweis von Rest-DNA gewähr leistet die Konsistenz zwischen den Produktions chargen und bietet eine Referenz für die Bewertung der Produkt qualität.
Zur Analyse der DNA-Konzentration und Größen verteilung von Wirtszellen werden zunächst DNA-Fraktionen aus der Probe extrahiert, um den Nachweis ohne inhibitor ische Verbindungen aus der Proben matrix sicher zustellen. Die magnetische Perlen trennung ist die am häufigsten verwendete Technologie für diesen Zweck und ermöglicht automat isierte Extraktion prozesse, die den Durchsatz und die Präzision erhöhen.
Um die Extraktion effizienz der verbleibenden Wirtszell-DNA zu bestimmen, wird der Probe vor der Extraktion eine bekannte Menge Ziel-DNA (das "Spike") zugesetzt. Durch Vergleich der gemessenen DNA-Menge nach der Extraktion mit der Spike-Menge kann die Extraktion effizienz berechnet werden. Dieser Effizienz wert wird dann verwendet, um die verbleibende Wirtszell-DNA in der Probe zu bestimmen. Eine Verringerung der Extraktion effizienz zeigt das Vorhanden sein von inhibitor ischen Verbindungen an, die mit der Nukleinsäure zusammen extrahiert wurden.
Die Entwicklung einer hoch empfindlichen und spezifischen Nachweis methode für Wirtszell-DNA unter Verwendung einer Echtzeit-PCR erfordert ein sorgfältiges Primer-Design und eine Optimierung der PCR-Reaktion. Die Spezifität und Sensitivität vonEchtzeit-PCRWerden durch Glüht emperatur, Zeit und die Konzentrationen von Kationen und Primern im Reaktions puffer beeinflusst. Das Anvisieren eines in mehreren Kopien vorhandenen Gens kann die Empfindlichkeit des Assays erhöhen.
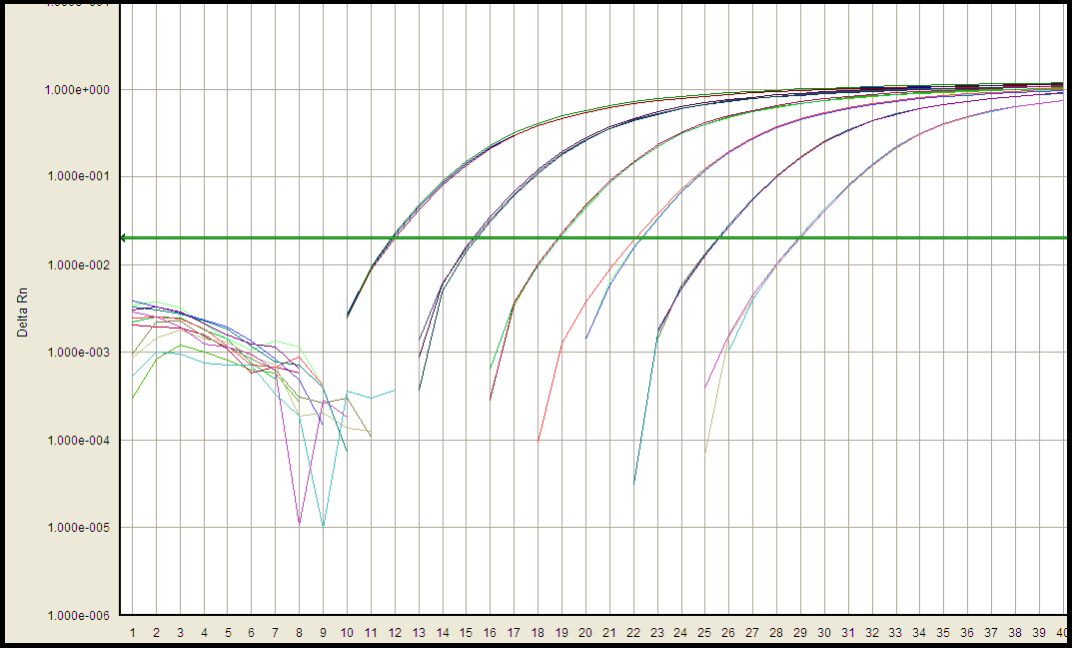
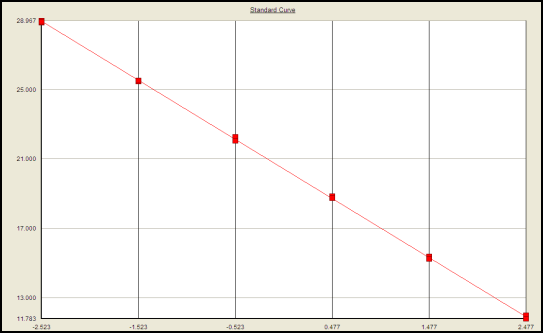
Die Linearität und der Bereich der Assay methoden wurden durch Berechnung der Regression linie der Standard kurve ausgewertet. Die Genauigkeit wurde bewertet, indem der Wiederherstellung prozentsatz von DNA-Standards mit Stacheln in drei verschiedenen Konzentrationen analysiert wurde. Intra-Assay-und Inter-Assay-Genauigkeit wurden über den %-CV aller QCs auf jeder Ebene bewertet. Die Empfindlichkeit wurde durch Überprüfung von LOD und LLOQ bestimmt. Die Spezifität wurde durch Analyse von DNA-Proben oder einem Pool von Matrix-DNA bewertet, die aus der relevanten Spezies/dem betreffenden Stamm extrahiert wurden. Die Robustheit wurde bewertet, indem die Stabilität der Assay leistung unter verschiedenen Lager bedingungen bewertet wurde.
Der Validierung umfang des verbleibenden Wirtszell-DNA-Assays umfasst:
Genauigkeit
Präzision
Spezifität
Grenze der Quant ifizierung (LOQ)
Linearität
Reichweite
Robustheit
Ein vollständig validierter Assay ermöglicht die Verwendung von im Handel erhältlichen Produkten oder speziell entwickelten Kits, die auf die Wirts-DNA-Sequenz abzielen, sodass er für Tests unter biologischen Produkten geeignet ist.
Fallstudie-DNA-Quant ifizierung der Rest wirts zelle
CHO HCD Validierung leistung-
Standard kurve: Verstärker effizienz 96,6%, Korrelation koeffizient 0,999